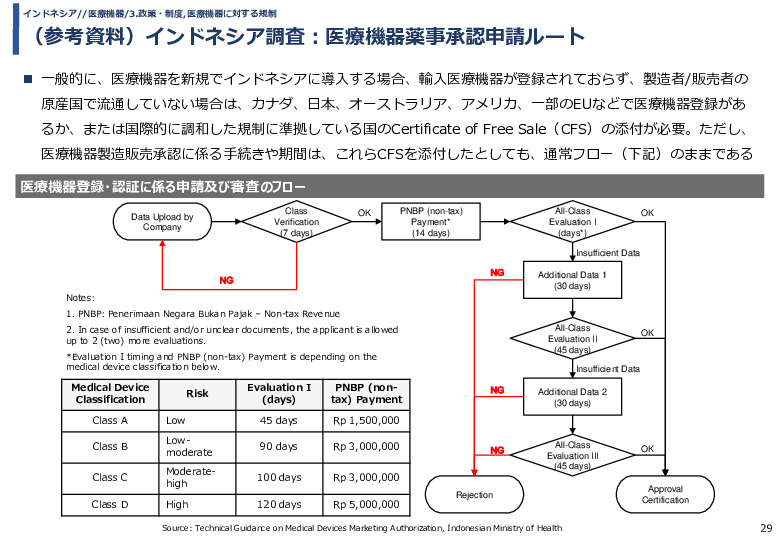
一般的に、医療機器を新規でインドネシアに導入する場合、輸入医療機器が登録されておらず、製造者/販売者の原産国で流通していない場合は、カナダ、日本、オーストラリア、アメリカ、一部のEUなどで医療機器登録があるか、または国際的に調和した規制に準拠している国のCertificate of Free Sale(CFS)の添付が必要。ただし、医療機器製造販売承認に係る手続きや期間は、これらCFSを添付したとしても、通常フロー(下記)のままである
よくある質問をご覧いただき、ご質問が解決しない場合は、下記お問い合わせフォームよりお問い合わせ下さい。

